Europska komisija objavila factsheet o primjeni nove Uredbe za procjenu zdravstvenih tehnologija
redba (EU) 2021/2282 Europskog parlamenta i Vijeća od 15. prosinca 2021. o procjeni zdravstvenih tehnologija i izmjeni Direktive 2011/24/EUa se primjenjuje od 12. siječnja 2025. godine.
Ona navodi kako je razvoj zdravstvenih tehnologija ključan pokretač gospodarskog rasta i inovacija u Uniji i od ključne je važnosti za ostvarenje visokog stupnja zaštite zdravlja koji zdravstvene politike trebaju osigurati za dobrobit svih.
Zdravstvene tehnologije predstavljaju inovativan gospodarski sektor i čine dio cjelokupnog tržišta troškova zdravstvene zaštite koji iznose 10 % bruto domaćeg proizvoda Unije. Zdravstvene tehnologije obuhvaćaju lijekove, medicinske proizvode, in vitro dijagnostičke medicinske proizvode i medicinske postupke te mjere za sprečavanje, dijagnosticiranje ili liječenje bolesti.
Procjena zdravstvenih tehnologija postupak je koji se temelji na znanstvenim dokazima, a kojim se nadležnim tijelima omogućuje određivanje relativne djelotvornosti novih ili postojećih zdravstvenih tehnologija. Procjena zdravstvenih tehnologija posebno je usmjerena na dodanu vrijednost pojedine zdravstvene tehnologije u usporedbi s novim ili postojećim zdravstvenim tehnologijama. Procjena zdravstvenih tehnologija može doprinijeti promicanju inovacija kojima se pacijentima i društvu u cjelini nude najbolji ishodi te je važan alat za osiguranje ispravne primjene i upotrebe zdravstvenih tehnologija.

Procjenom zdravstvenih tehnologija mogu se poboljšati znanstveni dokazi koji se upotrebljavaju u donošenju kliničkih odluka i pristup pacijenata zdravstvenim tehnologijama, uključujući slučajeve u kojima pojedina zdravstvena tehnologija postane zastarjela. Ishodi procjene zdravstvenih tehnologija upotrebljavaju se za pružanje podataka u svrhu donošenja odluka koje se odnose na dodjelu proračunskih sredstava u području zdravstva, na primjer u pogledu određivanja cijena ili razina naknada za zdravstvene tehnologije. Procjena zdravstvenih tehnologija stoga može pomoći državama članicama u stvaranju i očuvanju održivih sustava zdravstvene zaštite te poticati inovacije koje osiguravaju bolje ishode za pacijente.
Ovom Uredbom nastoji se postići visoka razina zaštite zdravlja pacijenata i korisnika te istodobno osigurati neometano funkcioniranje unutarnjeg tržišta u pogledu lijekova, medicinskih proizvoda i in vitro dijagnostičkih medicinskih proizvoda. Ovom se Uredbom istodobno uspostavljaju okvir za potporu suradnji država članica i mjere potrebne za kliničku procjenu zdravstvenih tehnologija. Oba se cilja nastoje postići istodobno te su neodvojivo povezani i jednako važni. Ovom se Uredbom istodobno nastoji pružiti visok stupanj zaštite zdravlja i omogućuje suradnja među državama članicama na određenim aspektima procjene zdravstvenih tehnologija. Zajednički rad trebao bi se odvijati u skladu s načelom dobre administrativne prakse i trebao bi biti usmjeren na postizanje najviše razine kvalitete, transparentnosti i neovisnosti.
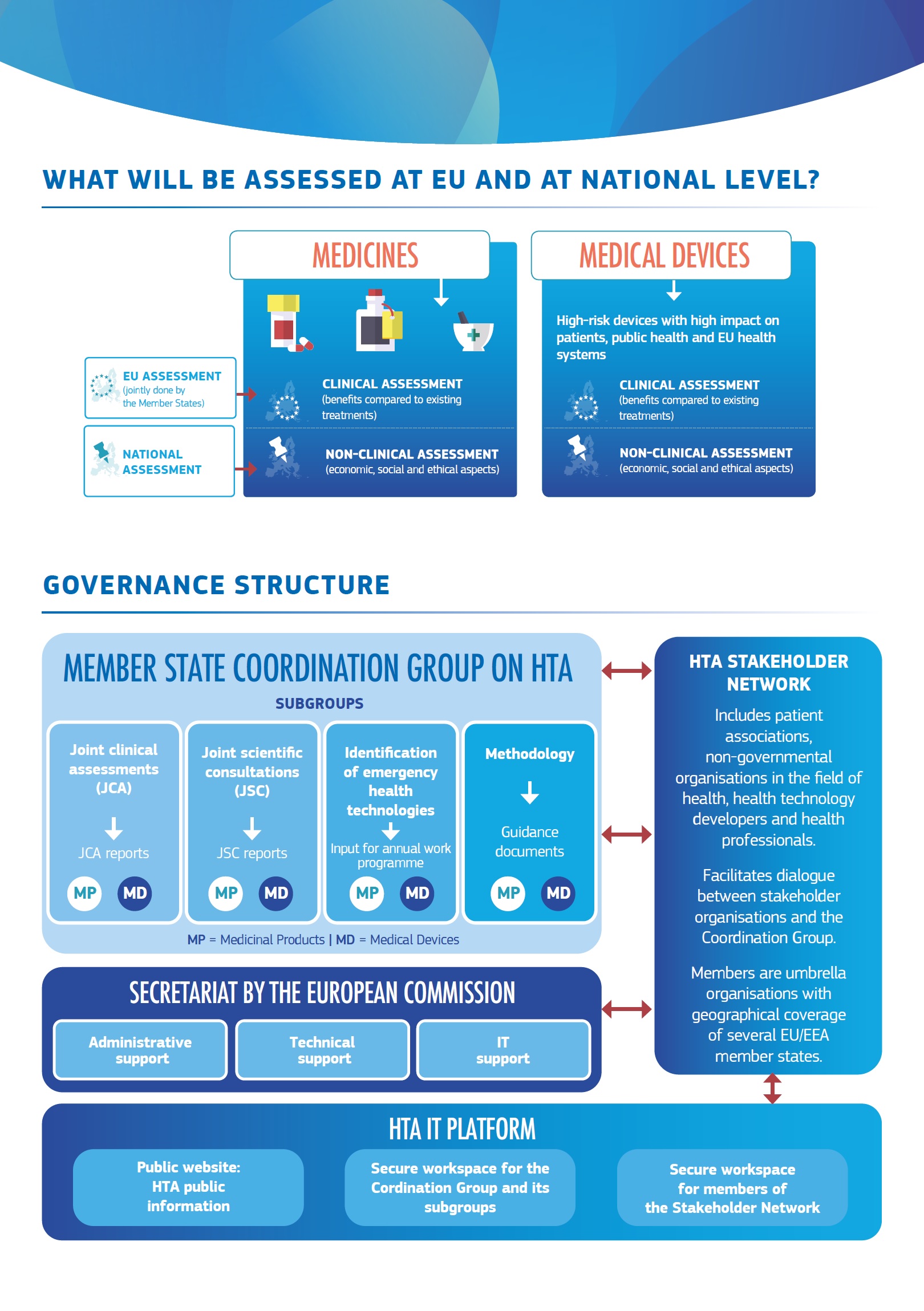
S Vama dijelimo najnoviji update o Uredbi za procjenu zdravstvenih tehnologija koji je objavila Europska komisija.



REFERENCES //
https://health.ec.europa.eu/health-technology-assessment/regulation-health-technology-assessment_en
https://health.ec.europa.eu/system/files/2023-05/hta_regulation-implementation_factsheet_en.pdf





